摘要:综合基因组图谱的使用,特别是F1CDx,可根据RECIST标准选择一种靶向治疗,以快速控制肿瘤及其转移。该病例表明,拉罗替尼不仅对NTRK融合有效,而且可能对NTRK基因扩增有效。
NTRK基因融合是已知的重要致癌和具有转化潜力的分子之一。因此,NTRK基因融合正在几种肿瘤类型中作为癌症治疗的靶点进行研究。关于NTRK基因融合的治疗,已经开发了几种TRK抑制剂,包括拉罗替尼(larotrectinib)。拉罗替尼是一种可口服的TRK受体家族选择性抑制剂,近年来在NTRK基因融合的儿童和成人患者中显示出显著的临床疗效,目前已获欧盟和美国批准。NTRK基因扩增已证明导致TRK过表达。然而,针对NTRK基因扩增的靶向治疗效果的研究尚不多见。在本病例报告中,我们报告了一例NTRK1基因扩增的转移性鳞状食管癌患者,他接受了拉罗替尼靶向治疗。
荧光原位杂交(FISH)检测显示患者没有出现NTRK融合,但出现了NTRK1扩增。初诊时,患者表现为食管中段肿瘤梗阻,同时伴有肝、肺转移,UICC IV期,WHO表现状态3。该例NTRK1基因扩增的转移性食管癌患者,接受了拉罗替尼靶向全身治疗。患者口服拉罗替尼标准剂量2 × 100 mg,治疗期间未发生副作用。
原发性肿瘤和肝脏病变同时活检确定了转移性鳞状细胞食管癌。从肝转移瘤中获得的全面基因组图谱发现了大量的基因组改变,包括NTRK1扩增。由于患者的表现状态下降,无法进行化疗。虽然拉罗替尼只被批准用于NTRK基因融合的癌症治疗,但根据RECIST标准,给药拉罗替尼治疗开始后6周内,食管胃十二指肠镜检证实原发肿瘤缩小,食管再活检无肿瘤(图1)。十二指肠黏膜、胃窦黏膜没有形态学上的病理发现。通过胸部和腹部CT进行评估,显示多个肺转移伴随着肿瘤标志物(鳞状细胞癌(SCC))减少。目标病灶的最长直径之和下降到33mm,胸腔积液已经消退。肝转移伴肿瘤标志物减少,在随后的肝活检中,NTRK1基因扩增低于检测限度。
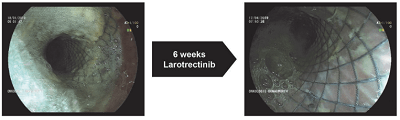
图1 左为接受拉罗替尼治疗前,右为接受拉罗替尼治疗6周后
随着拉罗替尼(larotrectinib)、恩曲替尼(entrectinib)和塞曲替尼(selitrectinib),三种TRK抑制剂研发及上市,已为众多患者带来获益。虽然larotrectinib和entrectinib在NTRK基因融合中的活性已经确定,但它们在NTRK扩增中的作用尚不清楚。在一项多中心、开放标签、I期剂量递增研究中,调查了larotrectinib在成人实体肿瘤患者中的应用,其中1例患者为NTRK1基因扩增,larotrectinib有部分应答,这是决定治疗的依据。此患者有一个单一的小靶点病变(11mm),缩小了5mm(45.5%),缓解持续时间为3.7个月,这与本文所述患者观察到的缓解结果相似。本文患者,在使用拉罗替尼治疗后肿瘤显著缩小,根据RECIST标准分类为部分缓解。
综上,综合基因组图谱的使用,特别是F1CDx,可根据RECIST标准选择一种靶向治疗,以快速控制肿瘤及其转移。该病例表明,拉罗替尼不仅对NTRK融合有效,而且可能对NTRK基因扩增有效。
2025-09-26 11:16:07
2025-09-26 11:12:42
2025-09-26 11:06:50
2025-09-26 11:01:18
2025-09-26 10:58:00
2025-09-26 10:46:03
2025-09-26 10:35:28
2025-09-26 10:31:19
2025-12-09 22:34:23
2025-12-09 22:31:45