摘要:转移性乳腺癌试验背景DS8201的疗效在DESTINY-Breast01(NCT03248492)研究中进行了评估,这是一项多中心、单臂的试验,纳入了184名HER2阳性、不可切除和/或转移性乳腺癌的女性患者,她们之前接受过两种或两种以上的抗HER2治疗。在筛查时,排除有治疗ILD(间质性肺疾病)史或当前ILD史的患者。有临床意义的心脏病病史、活动性脑转移和ECOG体力状况评分表现状态>1的患者也
DS8201的疗效在DESTINY-Breast01(NCT03248492)研究中进行了评估,这是一项多中心、单臂的试验,纳入了184名HER2阳性、不可切除和/或转移性乳腺癌的女性患者,她们之前接受过两种或两种以上的抗HER2治疗。在筛查时,排除有治疗ILD(间质性肺疾病)史或当前ILD史的患者。有临床意义的心脏病病史、活动性脑转移和ECOG体力状况评分表现状态>1的患者也被排除在外。
患者每3周静脉注射5.4mg/kg的DS8201,直到出现不可接受的毒性或疾病进展。肿瘤成像每6周进行一次,脑转移患者在基线检查时必须进行脑部CT/MRI检查。主要疗效结果是通过独立中心审查(ICR)使用RECISTv1.1评估所确认的客观缓解率(ORR)和响应持续时间(DOR)。
在局部晚期/转移患者中,既往癌症治疗方案的中位数为5(范围:2-17)。所有患者均曾接受过曲妥珠单抗、阿多曲妥珠单抗和恩他辛治疗,66%的患者曾接受过培妥珠单抗治疗。
DESTINY-Breast01独立中心评价的疗效结果,确定客观缓解率(95%CI)为60.3%(52.9,67.4);完整应答为4.3%;部分应答为56.0%;持续应答的中位月数(95%CI)† 为14.8(13.8,16.9)
在DESTINY-Gastric01(NCT03329690)研究中评估了DS8201的疗效,这是一项在日本和韩国进行的多中心、开放标签、随机试验,招募了188名HER2阳性(IHC3+或IHC2+/ISH阳性的成年患者)、局部晚期或转移性胃或GEJ腺癌患者,之前至少接受过两种治疗方案(包括曲妥珠单抗、氟嘧啶和含铂化疗)并取得进展。
患者按2:1的比例随机分为两组,第一组每3周接受DS8201(N=126)6.4mg/kg静脉注射,另一组选择化疗:伊立替康(N=55)每2周静脉注射150mg/m2,或紫杉醇(N=7)每周静脉注射80mg/m2。随机分组按HER2状态(IHC3+或IHC2+/ISH+)、ECOG表现状态(0或1)和地区(日本或韩国)进行分层。肿瘤影像学评估在筛查时进行,从第一次治疗剂量开始每6周进行一次,治疗直到出现不可接受的毒性或疾病进展。主要疗效结果是意向治疗人群的客观缓解率(ORR)和总生存期(OS)。其他疗效结果包括无进展生存率(PFS)和DOR。
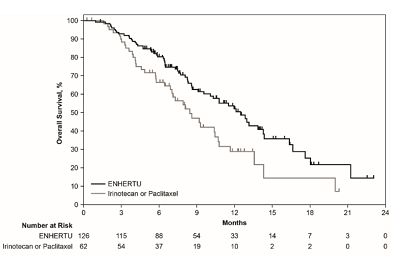
DS8201组的总生存率(OS)中位月数为12.5(9.6,14),伊立替康或紫杉醇组的中位月数为8.4(6.9,10.7),两组之间的危险比为0.59(0.39,0.88);DS8201的无进展生存率(PFS)为5.6个月,比伊立替康组高出2.1个月,两者的危险比为0.47(0.31,0.71);DS8201客观缓解率(ORR)为伊立替康组的7倍有余;DS8201的反应持续时间(DOR)为11.3(5.6,NR),伊立替康组为3.9(3.0,4.9)
DS8201和伊立替康/紫杉醇的总体存活率(OS)的Kaplan-Meier分析图如下:
注:本文仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。转载请注明出处。

 优赫得/德曲妥珠单抗(DS8201)
优赫得/德曲妥珠单抗(DS8201) 冻干粉
100mg
 英国阿斯利康
英国阿斯利康
靶向HER2的抗体和拓扑异构酶抑制剂的药物偶联物。
2025-10-01 18:01:43
2025-10-01 17:53:46
2025-10-01 17:19:20
2025-10-01 17:13:44
2025-10-01 17:05:17
2025-10-01 17:00:56
2025-10-01 16:47:52
2025-10-01 16:22:20
2025-05-22 14:49:28
2025-05-22 14:39:38