摘要:聚焦索托拉西布靶向治疗KRAS G12C阳性非小细胞肺癌
在非小细胞肺癌(NSCLC)患者中有13% 患者为KRAS密码子12突变。针对KRAS G12C突变的靶向治疗是具有挑战性的,这是因为GTP在细胞质中含量丰富,会快速水解,以及难以设计出足够浓度的药物小分子来抑制KRAS。基于临床前试验和临床试验结果,一种新型KRAS G12C抑制剂索托拉西布(AMG 510)于2021年5月年获得FDA批准,打破了KRAS靶点不可成药的魔咒。在这里,我们进一步详细探讨AMG 510的发展、疗效、临床试验及副作用,以求帮助更多患者获益。
2013年,Shokat等研究了以KRAS的半胱氨酸(Cys)12为靶点的共价抑制剂。ARS-1620是第一个在体内证明有效的共价KRAS G12C抑制剂。为了进一步改善,科学家研发出多种化合物,但是由于生物利用度低、效果差和/或不能完全限制键的旋转,新药研发很快就遇到了问题。此外,细胞内GTP含量丰富,产生了一个具有挑战性的环境。经过多次调整后,(R)-38化合物被重新命名为AMG 510。它能很好的崩解、代谢,具有中等渗透性和良好的口服生物利用度,证明了其良好的活性,最终被批准为索托拉西布(sotorasib)。
KRAS密码子12突变损害了GTP的水解,导致组成活性状态,促进细胞增殖。AMG 510与KRASG12C半胱氨酸残基结合,以锁定该蛋白的活性形式,抑制细胞增殖,促进细胞凋亡。这种残基在野生型KRAS中不存在,限制了脱靶效应。
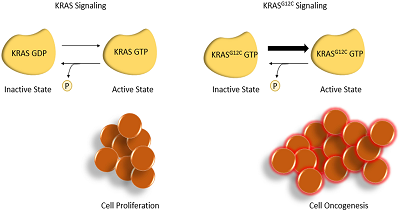
图1 KRAS G12C信号引起细胞突变
2021年5月,FDA基于CodeBreaK100研究批准了AMG 510用于治疗KRAS G12C突变的NSCLC。
CodeBreak 100多中心试验的I期部分评估了AMG 510在129入选患者中的应用。在NSCLC组中,包含了18岁或以上的局部晚期或转移性KRAS G12C NSCLC患者。主要终点是安全性,次要终点是药代动力学、客观反应率、反应持续时间 (DOR) 、疾病控制、无进展生存时间(PFS)和疾病稳定持续时间。在NSCLC组中,59例患者中有19例获得了明确的缓解,33例患者病情稳定。中位缓解时间为1.4个月,中位DOR为10.9个月,中位PFS为6.3个月。最常见的不良反应是腹泻和恶心。
CodeBreak 100多中心试验的II期部分共纳入126名受试者,根据I期临床试验结果,受试者每天接受960mg AMG 510治疗。试验结果表明AMG 510疗效显著,中位PFS为6.8个月 (95% CI: 5.1,8.2),客观缓解率为37.1%,在46例有客观缓解的患者中,4例完全缓解 (3.2%),42例部分缓解 (33.9%)。疾病控制率为80.6%,DOR为11.1个月,中位治疗时间为5.5个月,中位总生存期为12.5个月。临床试验反应出AMG 510长期生存获益优势。
在副作用方面,CodeBreak 100多中心试验的II期试验数据显示125例患者发生了不良事件 (99.2% )。最常见的是腹泻64例 (50.8%),恶心39例 (31%),疲劳32例 (25.4%),关节痛27例 (21.4%)。AST升高27例 (21.4% 例),ALT升高26例 (20.6% 例)。88例 (69.8% ) 患者发生了治疗相关的不良事件,其中1例为4级事件 (0.8% ),25例为3级事件 (19.8% )。
可见AMG 510的诞生不仅为医生提供了高级“武器”,更为患者带来了生的希望!期待AMG 510造福更多中国患者!

 索托拉西布
索托拉西布 片剂
120mg*240片(美国版)|120mg*240片(德国版)|120mg*56片(孟加拉珠峰版)|120mg*56片(老挝卢修斯版)
 美国安进
美国安进
KRAS G12C突变是一种常见的肺癌驱动基因,约占非小细胞肺癌(NSCLC)患者的13%。 目前,已经有两种针对KRAS G12C突变的靶向药物获得美国FDA的批准,分别是索托拉西布(sotorasib)和阿达格拉西布(adagrasib)。
2025-12-23 23:32:45
2025-12-23 23:30:18
2025-12-23 23:26:53
2025-12-23 23:22:34
2025-12-23 23:20:18
2025-04-24 15:17:10
2025-04-24 15:10:38
2025-04-24 15:04:37
2025-04-24 14:52:48
2025-04-24 14:44:33