摘要:德喜曲妥珠单抗的获批认证上市情况2019年12月,美国FDA加速批准德喜曲妥珠单抗上市,用于既往接受过抗HER2治疗方案的HER2阳性不可切除或者转移性乳腺癌/既往接受过一线或二线化疗的HER2低表达(定义为IHC1+/IHC2+且ISH阴性)的不可切除或转移性乳腺癌患者的治疗。2020年3月,德喜曲妥珠单抗在日本上市。2021年1月,德喜曲妥珠单抗在欧洲上市。2022年4月24日,德喜曲妥珠单抗
2019年12月,美国FDA加速批准德喜曲妥珠单抗上市,用于既往接受过抗HER2治疗方案的HER2阳性不可切除或者转移性乳腺癌/既往接受过一线或二线化疗的HER2低表达(定义为IHC1+/IHC2+且ISH阴性)的不可切除或转移性乳腺癌患者的治疗。2020年3月,德喜曲妥珠单抗在日本上市。2021年1月,德喜曲妥珠单抗在欧洲上市。2022年4月24日,德喜曲妥珠单抗也获得了中国国家药品监督管理局的“优先审评”,相信不久之后会在国内正式上市。
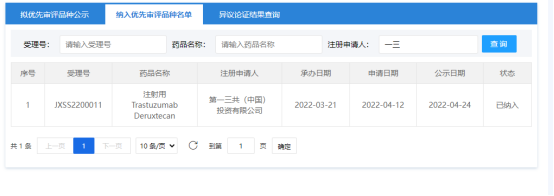
对于HER2阳性晚期乳腺癌,一线首选方案三药联用—化疗+曲妥珠单抗+帕妥珠单抗—的中位无进展生存期为18个月,二线治疗药物赫赛莱(T-DM1)的中位无进展生存期仅仅9个月,而单药德喜曲妥珠单抗的中位无进展生存期就达19.4个月。在最新2022版NCCN指南中,德喜曲妥珠单抗已颠覆了赫赛莱药物长达9年的首选地位,一跃成为HER2阳性晚期乳腺癌二线治疗的优选药物。
是一款靶向人表皮生长因子受体-2(HER2)的抗体偶联(ADC)药物,由两部分组成:第一部分是针对HER2靶点的抗体,可以精准识别并且结合此蛋白异常表达的肿瘤细胞;第二部分是毒性较强的化疗药物—伊立替康。这种设计会使抗体带着化疗药去精准定位肿瘤细胞,然后再高效地给这些细胞下毒,杀死它们。
比起前2代ADC药物,德喜曲妥珠单抗独特性主要表现在以下2个方面:第一是药抗比高,它的每个抗体分子可以携带8个细胞毒素,是赫塞莱的两倍!从而拥有极强的杀伤力。第二是膜渗透性高,这使其能渗透杀伤邻近的肿瘤细胞,这种“旁观者效应”使其对HER2高低表达的乳腺癌均有效。
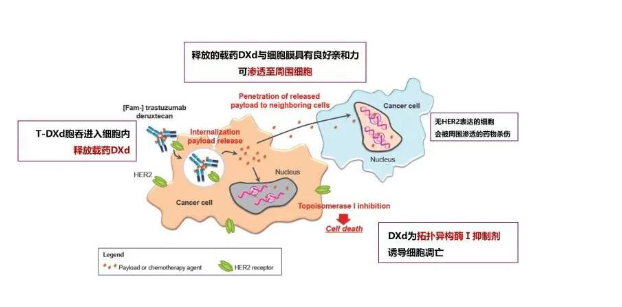
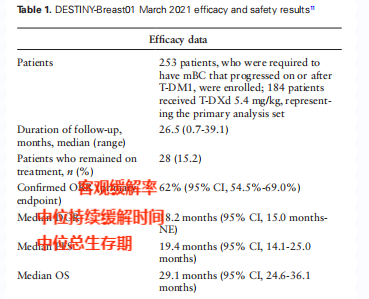
从 II 期开放标签 DESTINY-Breast01 试验(NCT03248492; DS8201-A- U201)开始,德喜曲妥珠单抗对经过大量预处理的HER2阳性复发转移性乳腺癌患者中显示出持久的高缓解率:
客观缓解率为62%,这意味着6成以上患者的肿瘤缩小了30%以上;
疾病临床进展为1.6%,这意味着184 名只有3 名患者病情发展或恶化了,而98.4%患者病情得到控制或稳定;
中位持续缓解时间为18.2个月,复发转移性乳腺癌患者处于稳定或持续缓解的状态达到一年半(缓解持续时间越长,患者最终的生存期越长);
中位总生存期19.4个月,代表着半数患者活过了一年半以上。
移至二线治疗,DESTINY-Breast03 ( NCT03529110)试验再续辉煌,德喜曲妥珠单抗创造了整个晚期乳腺癌领域中位无进展生存期(18.5个月)新的历史纪录。
在此之前,HER2靶向药物只对HER2高表达患者有效,而对HER2低表达无效。HER2低表达乳腺癌患者面对无靶向药可用的局面,德喜曲妥珠单抗的上市扭转了这一局面。它不仅对HER2低表达有效,而且是疗效显著。III 期 DESTINY-Breast04 试验的结果表明,手术/转移性 HER2低表达乳腺癌患者的无进展生存期延长了近一倍。对于这个结果,英国阿斯利康、日本第一三共发言人表示“德喜曲妥珠单抗即将成为HER2低表达肿瘤患者的首选方案,甚至可能会改写乳腺癌的分类和治疗手段。”
在一项德喜曲妥珠单抗对比化疗治疗 HER2-低表达晚期乳腺癌的成本效益研究中,德喜曲妥珠单抗可以为 HR+/HER2-低表达 晚期乳腺癌患者提供更多的健康益处。但与化疗相比,此药治疗的成本效益不高。该研究的主要负责人员朱博士还表示,她认为未来还可以研究德喜曲妥珠单抗的长期益处,需要更多的外部数据来验证模型相对延长的生存数据。

一项图卡替尼和德喜曲妥珠单抗联用疗效和安全性的研究(编号:NCT04539938)2020年首次发布,但实验结果目前仍无披露。
一项德喜曲妥珠单抗在新诊断或进展性脑转移的 HER2 阳性乳腺癌患者中的 II 期研究(编号:NCT04752059)尚在进行中,预计2023年完成。
一项德喜曲妥珠单抗和纳武单抗联合治疗已完成放化疗后食管切除术的 HER2 过表达食管胃腺癌患者的安全性和初步疗效的研究(编号:NCT05480384)刚在实验平台完成注册。
注:本文仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。转载请注明出处。
2026-03-17 22:06:52
2025-12-18 21:43:29
2025-12-18 21:35:40
2025-12-18 21:28:02
2025-12-18 21:24:06
2025-12-18 21:21:39
2025-12-18 20:23:21
2025-12-18 20:16:04
2025-12-18 20:08:03
2025-12-18 20:00:00